|
При пересаживании клеток нервного гребня в относительно раннем периоде их дальнейшее развитие может изменяться вплоть до того, что они могут в дальнейшем использовать абсолютно другой трансмиттер, например ацетилхолин, вместо норадреналина. В некоторых случаях такая смена медиатора происходит в ходе нормального развития. Например, симпатические нейроны, иннервирующие потовые железы, изначально синтезируют норадреналин, но в период между второй — третьей неделями постнатального развития факторы, выделяемые железой, приводят к тому, что они начинают вырабатывать ацетилхолин. На более поздних стадиях клетки нервного гребня становятся уже слишком зрелыми и теряют способность менять свою дифференцировку в соответствии с изменениями окружающей среды.
Изучение механизма смены трансмиттера проводилось на культурах клеток симпатических ганглиев. Когда нейроны выделялись из верхнего шейного ганглия новорожденного крысенка и вырашивались в культуре в отсутствие клеток других типов, они все содержали фермент тирозингидроксилазу, синтезировали и образовывали запасы катехоламинов. |
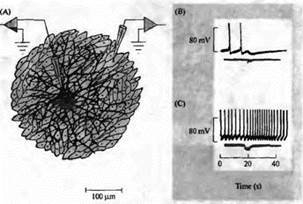
Рис. 7. Отдельные нейроны симпатических ганглиев способны выделять как ацетилхолин, так и норадреналин в синапсах на культуре клеток сердца. (А) Микрокультура, содержащая отдельные симпатические нейроны, выращенные на островке клеток сердечной мышцы. (В) Короткая серия импульсов в нейроне (10 Гц, показано в виде отклонений нижней записи) вызывает ингибирование спонтанной активности миоцита из-за высвобождения АХ (верхняя запись). (С) Добавление атропина (10--7 М) блокирует тормозный холинергический ответ, что приводит к проявлению возбуждающего эффекта, вызванного высвобождение норадреналина. |
|
Однако, если нейроны вырашивались в присутствии определенных типов ненейрональных клеток, таких как клетки сердечной мышцы или потовых желез, нейроны постепенно переставали синтезировать катехоламины и начинали синтезировать вместо этого фермент холинацетилтрансферазу и ацетилхолин. Для того, чтобы окончательно установить, что подобные изменения возможны в одиночных нейронах, они культивировались на микроостровках клеток миокарда (рис. 7). Нейроны быстро вытягивали свои отростки и образовывали синаптические контакты с клетками миокарда. Сначала эти синапсы были чисто адренергическими, затем, по прошествии нескольких дней, клетки начинали выделять вместе норадреналин и ацетилхолин. В конечном счете передача становилась полностью холинергической.
Фактор, который вызывал холинергическую дифференцировку симпатических нейронов, был выделен из среды клеток сердца и клонирован. Оказалось, что это фактор ингибирующий развитие лейкемии (leukemia inhibitory factor, LIF), белок, который ранее был описан по его способности индуцировать дифференцировку клеток иммунной системы. Два других близких цитокина, цилиарный нейротрофический фактор (ciliary neurotrophic factor, CNTF) и кардиотрофин-1, как было обнаружено, вызывают сходные эффекты в культуре нейронов. Все эти три фактора активируют рецепторный комплекс (называемый LlFR/3-gpl30 рецептор), блокирование которого угнетает развитие холинергических свойств нейронов, культивируемых вместе с клетками потовых желез. Однако иннервация потовых желез у мутантных мышей, не имеющих L1F и CNTF, формируется нормально, а результаты других экспериментов заставляют предположить, что кардиотрофин-1 не является фактором, который может вызывать переключение в клеточной иннервации потовых желез in vivo. Хотя еще не описано генетическое выключение всех трех генов, вполне возможно, что скоро будет описан новый, еще не идентифицированный фактор потовых желез, являющийся лигандом для LIFR-gpl30 рецептора.
|


